PVP聚维酮简介
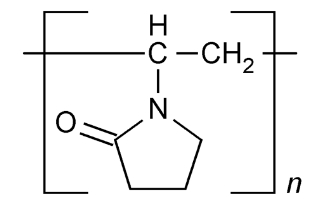
聚乙烯吡咯烷酮(PVP),是由N-乙烯基吡咯烷酮(NVP)线性聚合而成的水溶性高分子化合物,其分子结构式如图1.1所示。1938年,德国化学家Reppe首次用乙炔为原料合成PVP。到目前为止,PVP已发展成为非离子、阳离子、阴离子3大类,工业级、医药级、食品级3种规格,相对分子质量从数千至一百万以上的均聚物、共聚物和交联聚合物系列产品,并以其优异独特的性能获广泛应用。PVP不仅具有水溶性高分子的一般性质,如胶体保护作用、成膜性、黏结性、吸湿性、增稠性、凝聚作用以及与某些化合物的络合能力等,而且以优异的的溶解性和生理相容性,受到人们的重视青睐。在合成的高分子产品中,像PVP这样既溶于水,又溶于大部分有机溶剂,毒性极低,生理惰性相容性好的品种十分少见。
PVP因其优异的性能,受到了人们越来越多的关注,并在医药、食品、化妆品、水处理、纳米技术等这些与人们健康、科技发展密切相关的领域中获得越来越多的应用。
pvp聚维酮基础介绍
PVP的基本物理性质
市售PVP是白色、乳白色或者略带黄色的固体颗粒粉末。PVP具有良好的水溶性,其在水中的溶解过程是一个放热的过程,溶解热为-4.8×103J/mol。PVP固体的密度为,折光率。
PVP的堆密度与其分子量及生产工艺过程中的干燥方法有着密切的关系。一般来说,对于市售的固体PVP颗粒,其堆密度与分子量、干燥方法、颗粒大小有关,一般的堆密度可以通过以下公式(4.1)计算:
式中:dv——PVP的堆密度(g/ml);
M——PVP的质量(g);
Vp——PVP的堆体积(ml)。
PVP的分子量通常用K值来表示,据德国BASF公司报道:当K值<30时,其堆密度为0.4~0.6g/ml,当K值大于90时,其堆密度为0.11~0.25g/ml,不溶性PVP则为0.28~0.38g/ml。美国ISP公司报道,其PVP当K值为30时的堆密度为0.3g/ml。由此可见,当生产工艺及干燥方法改变时,PVP的堆密度会有较大的变化,不同厂家之间的同分子量PVP在堆密度方面也会存在一定的不同。另外,测定方法的不同也会导致PVP堆密度数据的差异。
但总体上可以看出,随着PVP分子量的增大,其堆密度越小,这是因为PVP分子量越大,其接枝程度越高,分子链越长,PVP分子堆积在一起时相互之间的空隙就越大;反之,分子量越小,PVP分子堆积在一起时相互之间的空隙就越小,进而使其有较高的堆密度。颗粒大小对PVP的堆密度也有着直接的影响,颗粒越大,颗粒间空隙越大,一定质量下的PVP堆体积就越大,由公式(4.1)可以看出,颗粒越大,PVP的堆密度就越小。
PVP分子量测定及其表征
成品PVP按分子量大小分成若干等级,一般用Fikentscher公式的K值来表示,K值是通过测定一定浓度的PVP水溶液的相对黏度,采用Fikentscher公式计算得到的,是不随PVP溶液的浓度而改变的常数。测定K值的常用方法是乌氏毛细管黏度计法测得PVP水溶液的相对黏度η,通过Fikentscher公式计算K值如下:

式中:K,K0——Fikentscher常数;
K——1000K0;
C——100ml溶液中溶解的PVP克数,通常为5,1或0.1;
PVP的K值与分子量之间并没有显著的函数关系,如图2.1所示:
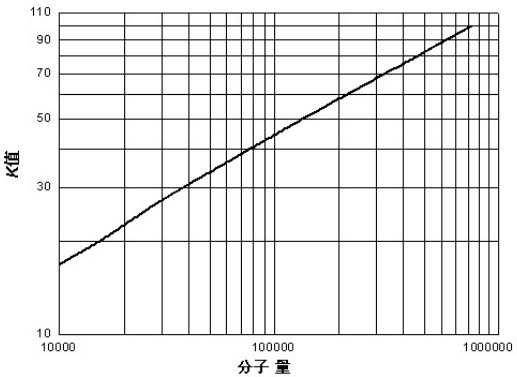
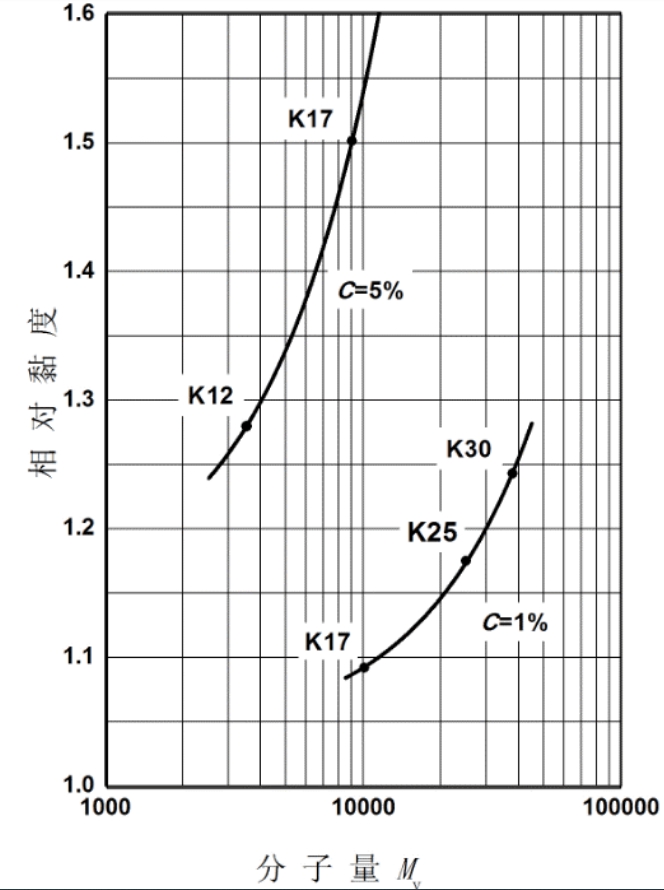
同样也可以将相对黏度与分子量直接相关联作曲线,结果如图2.2。可以在直接测得相对黏度后,直接从曲线上读出PVP的分子量。
相对黏度与分子量的关系
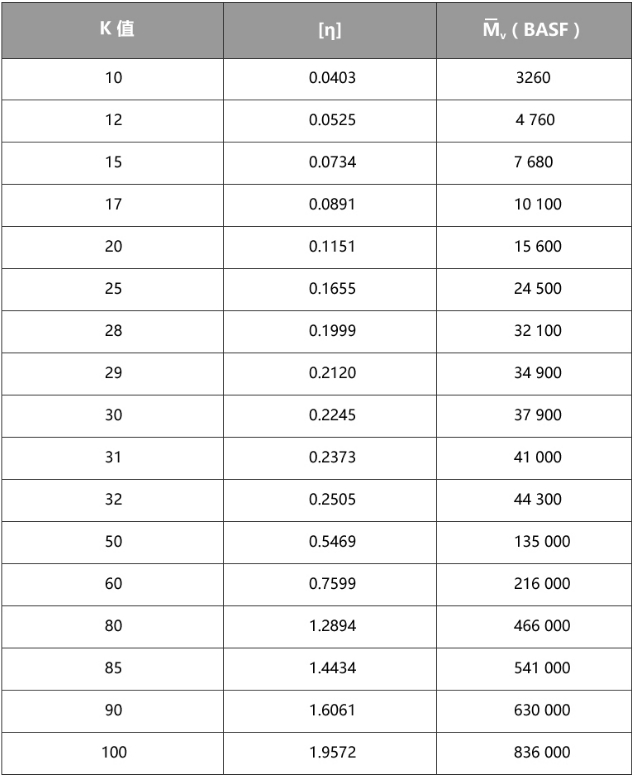
从上述论述中,我们可以发现,PVP的K值、特性黏度[η]、分子量有着一一对应的关系,它们之间的具体关系见表2.1。
表2.1PVPK值与特性黏度[η]和分子量之间的关系
重均分子量是通过测定分子重量的方法测定的,例如用超滤法或光衍射法测定的;数均分子量使用测定分子数量的方法测定的,如渗透压法和端基分析法确定。同时我们用来表征分子量的分散程度,即为分散系数,系数越大说明分子量的分布越宽,越分散。PVP的重均分子量与数均分子量与K值的关系间表2.2。
表2.2不同K值PVP的分子量对照
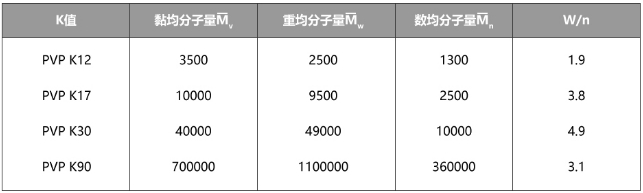
上表中的K值对应的黏均分子量与表2.1中所列有一定的区别,这是因为上述数据都是对市售产品为样品而测得,与推导公式时的实验室样品有一定的差异。某一标示K值的商品PVP,其实际分子量大都分布在其名义值两侧的一定范围内。此外,聚合方法的不同,乃至某一条件的细微改变、产品纯化方法、干燥工艺、分子量的测定方法和条件的不同都会导致测定结果的不同。
PVP光谱特性
Simonelli及其合作者,和Sekikawa及其合作者都对PVP的X-射线衍射结构作了研究,结果所得的散射角2θ分别为10°~26°和10°~40°,这些数据都表明PVP的结构是无定型非晶态结构,这一结论在目前被较为普遍的接受。
PVP的红外光谱可以通过两种方法测得,一是采用KBr压片,二是将PVP水溶液洒在AgCl圆盘上形成PVP的薄膜,然后测定。各种方法得到的PVP红外光谱大同小异,只是当PVP含杂质太多或有可以与PVP分子发生相互作用的分子时,PVP的红外光谱可能会出现较大的偏差。另外,共聚PVP和交联PVP红外光谱,由于共聚单体的不同或者交联剂分子结构的不同而不同。均聚PVP的红外光谱如图5.1所示。
图5.1PVP的红外光谱(KBr压片法,为10000)
由图谱可见,PVP的红外吸收峰较多,从500cm-1波数左右到3500cm-1波数都有吸收峰、其特征吸收带为—C=O伸缩振动跃迁产生的谱带,这一谱带的中心位置为1660~1680cm-1范围内,根据PVP的分子量大小等因素的变化,这一谱带的中心位置会存在不同程度的差异。另一方面,从PVP的红外谱图可以看出,—C=O伸缩振动谱带宽度约为30~35cm-1,数值偏大,说明—C=O与—C—N—酰胺键之间存在很强的作用力,相互之间发生了较强烈的耦合作用。在光谱图上,1300cm-1左右处为PVP分子的—C—N—的伸缩振动谱带,由此峰可定量推算PVP的含量。而3000~3500cm-1之间的强而宽的吸收带被公认为PVP中水分的吸收峰,这类水分是被PVP分子吸附的水分。此处峰值往往超过与其临近的在2900~3000cm-1的—C—H—伸缩振动谱,这正好与具有吡咯烷酮环的其他低分子化合物如NVP、乙基吡咯烷酮等相区分,后者不具备吸收水分的性质。利用这一点可以通过红外吸收光谱来定性或半定量的判断NVP的聚合反应转化率或者PVP溶液与NVP。
PVP的紫外吸收光谱如图5.2所示。
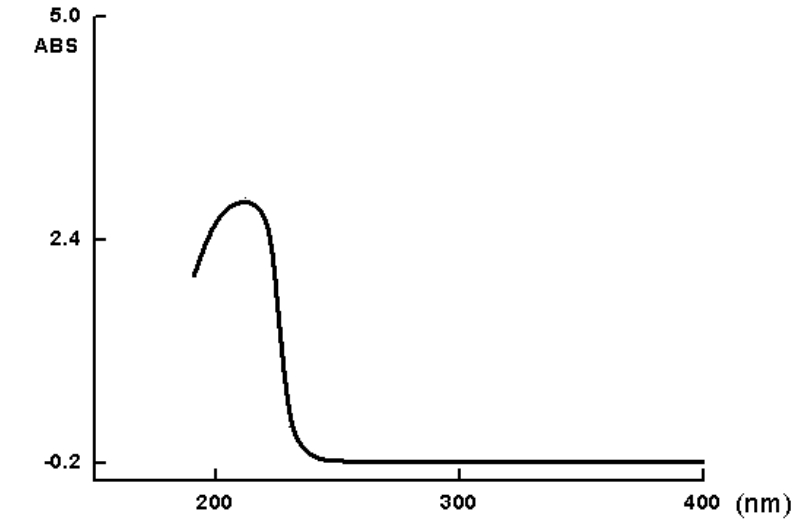
图5.2PVP紫外光谱图



