导读
近日,北京大学药学院化学生物学中心焦宁课题组提出了一种新颖而有效的方法,利用碘催化环丁烯酮的氧化重排反应,合成了呋喃-2(5H)-酮。值得注意的是,这种方法使用二甲基亚砜(DMSO)作为更绿色的氧化剂和氧气来源。反应在催化量的碘的作用下顺利进行,以良好的产率生成内酯。与依赖过氧酸或过氧化氢的传统Baeyer-Villiger氧化反应相比,DMSO的使用提供了一种更安全、更通用的替代方法。相关研究成果发表在Green Chemistry.上(DOI: 10.1039/d3gc01756g)。
研究背景
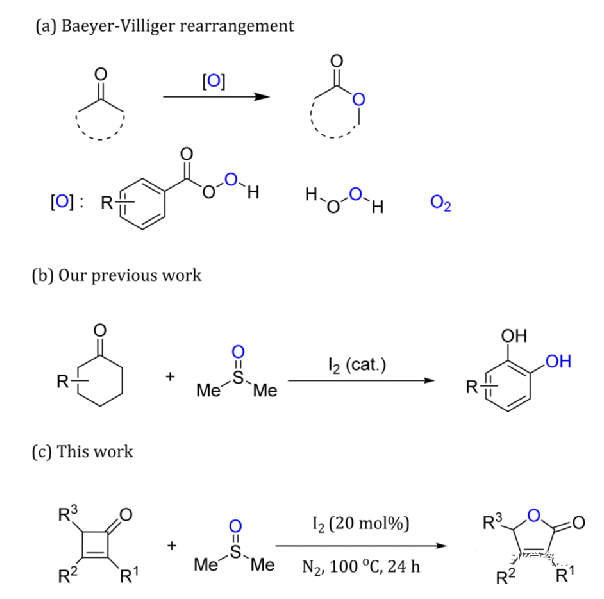
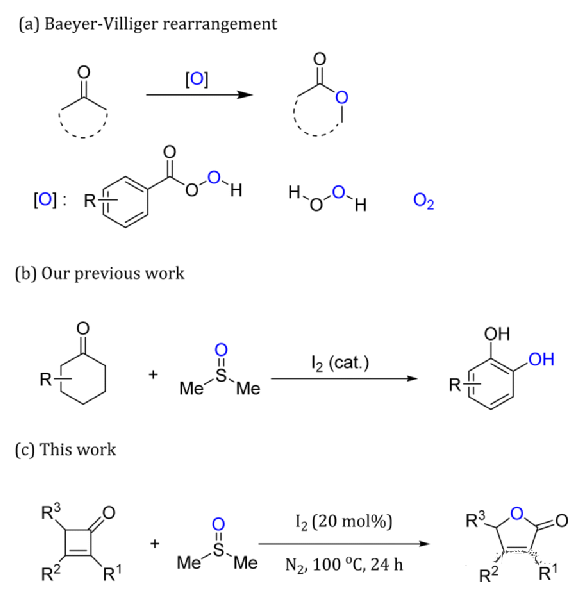
内酯,特别是γ-内酯骨架是一种用途广泛的结构,广泛存在于生物活性分子、药物和天然产物中(方案1)此外,γ-内酯可以作为合成γ-氨基酸的重要中间体,在药物活性化合物中普遍存在。因此,已经开发了许多内酯合成方法。在这些方法中,Baeyer-Villiger氧化法已被证明是制备和工业化生产内酯的有效方法(方案2a)。因此,已经开发了包括过氧酸在内的各种氧化剂和催化剂来促进这种转化。它们中的大多数需要使用强的或不稳定的氧化剂,如过氧化氢或过氧酸。因此,使用更安全、更温和、更容易获得的氧化剂和氧源将酮转化为内酯仍然是一个具有挑战性和可取的目标。
二甲基亚砜(DMSO)是工业上用二氧化氮或氧气氧化二甲基硫醚生产的,并已广泛用于有机化学。除了是一种廉价和低毒的溶剂,特别是在氧化体系中, DMSO已被广泛用作众所周知的命名反应中的氧化剂,如Swern氧化和PwiznerMoffatt氧化DMSO中氧原子的亲核性质使其成为有机反应中的常见氧源,包括Kornblum反应尽管有显著的进步作为我们开发氧化过程新方法的努力的一部分,作者报告了利用DMSO作为溶剂、氧化剂和氧源将环己酮直接转化为邻苯二酚(方案2b),从这一反应中得到灵感,设想DMSO可以在Baeyer-Villiger反应中作为过氧酸或过氧化氢的潜在替代品。在这项研究中,作者描述了在氮气气氛下,以二甲基亚砜为氧化剂和氧源,I2催化的环丁烯酮氧化重排反应合成取代呋喃-2(5H)-酮(方案2c)。使用简单易得的I2催化剂,并以二甲基亚砜为唯一试剂,使该方法相容、经济、安全,为合成γ-内酯提供了一种潜在的替代方法。
研究内容
作者首先以2-丁基-3-苯基环-2-烯-1-酮(1a)为模型底物,N-溴代丁二酰亚胺(NBS)为催化剂,DMSO为溶剂进行反应。在掌握了优化的反应条件后,作者探索了该反应的适用性。
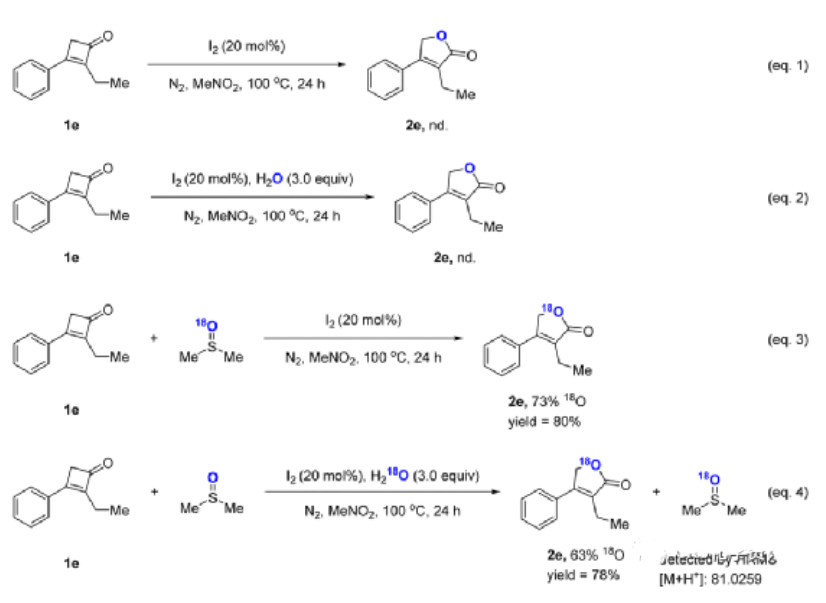
为了进一步了解反应机理,作者进行了一系列的实验研究。在标准条件下,环-2-烯-1-酮1e与DMSO的反应没有得到所需的产物(方案3,方程(1))。使用H2O而不是DMSO的系统也不起作用(方案3,等式(2))。此外,当1e与18O标记的DMSO反应时,以73%的产率获得了18O标记的产物18O-2e以及7%的氧同位素交换产物2e(方案3,式n(3))。相反,当在3.0当量的H218O存在下进行1e的反应时,以78%的产率得到了2e,其中63%是18O标记的产物(方案3,式n(4))。此外,反应混合物的HRMS分析表明有18O标记的DMSO的生成。这些结果表明,内酯产物中的额外氧原子来自DMSO,可能参与了H218O与DMSO之间的氧交换。
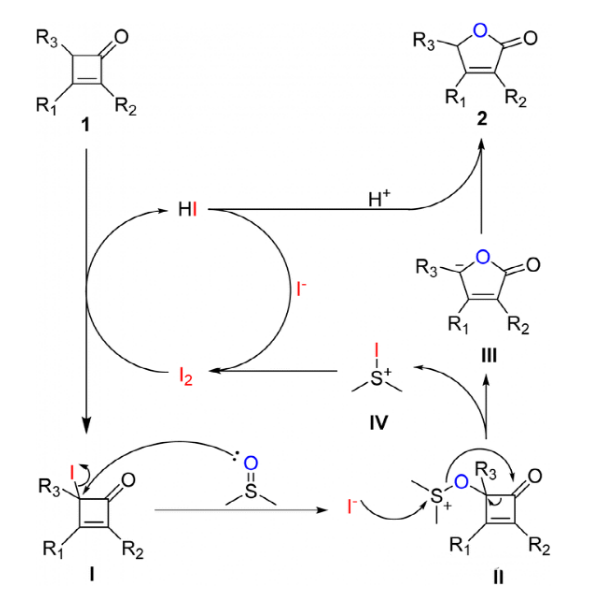
尽管该方案的作用机理尚不完全清楚,但在方案4的基础上提出了一个可行的催化循环最初,底物1被I2亲电卤化,导致4-碘-2-环丁烯酮I的生成,该反应在该催化体系中不稳定。随后,二甲基亚砜的氧原子对I进行亲核攻击,生成离子对中间体II。随后,中间体II发生氧重排,随后发生质子化,形成最终产物2。同时,生成的二甲基硫碘IV与I−发生氧化还原反应,再生I2,使其参与随后的催化循环。
总结展望
综上所述,作者成功地开发了一种新的、高效的氧化重排方法,用于从环丁烯酮选择性合成呋喃-2(5H)-酮。该过程中使用的催化剂是简单的I2,而DMSO既是氧源又是氧化剂。通过这个策略,可以合成一系列呋喃-2(5H)-酮。作者所在课题组目前正在对底物范围进行进一步的研究,并基于这一实用有效的方法探索合成应用。



