聚乙烯咪唑/聚乙烯吡咯烷酮
聚乙烯基咪唑/聚乙烯吡咯烷酮(PVI/PVP)的COEI-1-PVIPVP吸附剂共聚物
CAS:87865-40-5
1.对象、来源和适用范围
PVI/PVP吸附剂共聚物是不溶的微吸湿性粉末。它们是由N-乙烯基咪唑(化学文摘社编号:1072-63-5)和N-乙烯基-2-吡咯烷酮(化学文摘社编号:88-12-0)以9:1的比例聚合而成。N,n-二乙烯基咪唑烷-2-酮(化学文摘社编号13811-50)用作交联剂,其用量低于单体总量的2重量%。
PVI/PVP吸附性共聚物按照OIV酒类行为规范中描述的文件添加到葡萄汁或葡萄酒中,添加量低于500毫克/升。
PVI/PVP吸附性共聚物可以添加到葡萄汁或葡萄酒中,以防止由过量金属含量引起的缺陷或降低不期望的高金属浓度。
葡萄汁或葡萄酒必须通过孔径不超过3微米的过滤介质过滤,过滤压力不超过0.8巴。
2.同义词
1-乙烯基咪唑、1-乙烯基吡咯烷酮和1,3-二乙烯基咪唑烷酮的三元共聚物。
乙烯基咪唑/乙烯基吡咯烷酮交联共聚物。
3.贴标签于
标签必须注明PVI/PVP吸附共聚物用于酿酒。还必须注明储存和安全条件。
标签上必须注明3年有效期。
4.特性
白色至黄色粉末。
PVI/PVP吸附共聚物几乎不溶于目前所有的溶剂。因此不可能测量分子量。

质检单
检验项目 inspection item | 标准规定 standard code |
外观性状 external properties | 本品为白色或类白色粉末 This product is white or white powder |
干燥失重/% loss on drying/% | 5.0 |
炽灼残渣/% residue on ignition/% | ≤0.02 |
水溶物/% hydrotrope/% | ≤0.5 |
重金属/ppm heavy metal/ppm | ≤10 |
砷/ppm arsenic/ppm | ≤2 |
N-乙烯吡咯烷酮/ppm N-vinylpyrrolidone/ppm | ≤5 |
N-乙烯咪唑/ppm N-vinylimidazole /ppm | ≤10 |
含氮量/% nitrogen content/% | 26.0-29.0 |
*总菌落数 CFU/g Total colony number CFU/g | ≤100 |
| *霉菌和酵母菌数CFU/g Mold and yeast number CFU/g | ≤100 |
*金黄色葡萄球菌CFU/g Staphylococcus aureus CFU/g | 不得检出 not detectable |
| *沙门氏菌CFU/g Salmonella CFU/g | 不得检出 not detectable |
| *绿脓杆菌 CFU/g Pseudomonas aeruginosa CFU/g | 不得检出 not detectable |
| *大肠杆菌 CFU/g E. coli CFU/g | 不得检出 not detectable |
注:以上打*号项目执行随机测试。 Note: The above items marked with * were randomly tested.
试验
5.1. 干燥损失
给直径50毫米的金属胶囊去皮。将0.8至1.4克PVI/PVP吸附剂共聚物放入容器中,预先均化并在封闭天平中精确称重。在140°C±5°C的干燥箱中干燥1小时。让其在干燥器中冷却。再次称重。
干燥损失必须小于5 %。
5.2. 灰
将瓷坩埚加热至暗红色;让其在干燥器中冷却并称重。将1.5g PVI/PVP吸附剂共聚物放入坩埚中,并在800℃±25℃的马弗炉中以恒重焚烧,每次焚烧后让坩埚在干燥器中冷却,第一次焚烧持续时间为6小时。如有必要,预先焚化样品。
灰分的重量必须小于0.02 %。
5.3. 测试溶液的制备:
称量灰分后,将其溶解在1毫升浓盐酸(R)和10毫升蒸馏水中。加热以激活溶解。用蒸馏水补足20毫升。1毫升该溶液含有0.075克PVI/PVP吸附剂共聚物的矿物质。
5.4. 锌
使用第5.3点中制备的测试溶液,根据第二章中描述的方法测量锌。
锌含量必须低于1毫克/千克。
5.5. 熨斗
使用第5.3点中制备的测试溶液,根据第二章中描述的方法测量铁。
铁含量必须低于5毫克/千克。
5.6. 铜
使用第5.3点中制备的测试溶液,按照第二章中描述的方法测量铜。
铜含量必须低于1毫克/千克。
5.7. 铅
使用第5.3点中制备的试验溶液,根据第二章中描述的方法测量铅。
铅含量必须低于2毫克/千克。
5.8. 镉
使用第5.3点中制备的试验溶液,根据第二章中描述的方法测量镉。
镉含量必须低于1毫克/千克。
5.9. 砷
不要将溶液用于第5.3点中制备的试验。
按照第二章所述的方法测定砷。
砷含量必须低于2毫克/千克。
5.10.汞
不要将溶液用于第5.3点中制备的试验。
根据第二章中描述的方法测定汞。
汞含量必须低于1毫克/千克。
5.11.有机杂质
根据附录1中描述的方法测定有机杂质。
有机杂质的限值必须如下:
乙烯基吡咯烷酮的含量必须低于5毫克/千克
乙烯基咪唑的含量必须低于10毫克/千克
二乙烯基咪唑烷酮含量必须小于2毫克/千克
吡咯烷酮含量必须低于50毫克/千克
咪唑含量必须低于50毫克/千克
5.12.总氮的测量
将大约450毫克PVI/PVP吸附共聚物(测试部分m mg)在矿化烧瓶中,加入10 g密苏里催化剂[1]和3颗玻璃珠。用少量硫酸(R)清洗所有附着在瓶颈上的颗粒。总共添加20 ml硫酸(R ),沿着烧瓶壁流动,并通过旋转混合内容物。根据第二章中描述的方法继续分析。
相对于干重,总氮含量必须在26.0%和29.0%之间。
5.13.在水介质中的溶解度
将10g PVI/PVP吸附剂共聚物放入装有100 ml水的200ml刻度烧瓶中。摇动瓶子,让里面的东西静置24小时。在具有2.5微米直径孔的滤膜上过滤,然后在具有0.8微米直径孔的滤膜上过滤。水浴上蒸发滤液后剩余的干残渣必须少于0.5%。
5.14.在酸和醇中的溶解度
将1g PVI/PVP吸附剂共聚物加入到含有500 ml以下混合物的瓶中:
乙酸
3 g
乙醇
10毫升
水
100毫升
允许休息24小时。在具有2.5微米直径孔的滤膜上过滤,然后在具有0.8微米直径孔的滤膜上过滤。在水浴上浓缩滤液。在直径为70毫米的校准硅胶囊中的水浴上完成蒸发。考虑到500 ml乙酸、乙醇和水混合物蒸发后的所有残留物,蒸发后剩余的干残留物必须少于1%。
5.15.葡萄汁和葡萄酒中单体的测定及含量
5.15.1. 分析法
根据附录2中的分析方法进行测定
5.15.2. 葡萄汁和葡萄酒中单体的限量[2]
乙烯基吡咯烷酮的含量必须低于10微克/升
乙烯基咪唑含量必须低于10微克/升
吡咯烷酮含量必须低于25微克/升
咪唑含量必须低于150微克/升
储存;储备
PVI/PVP吸附共聚物必须保存在阴凉的地方。容器必须干燥且密封。
附录1用气相色谱法测定组成单体
和/或容易在乙烯基吡咯烷酮-乙烯基咪唑(乙烯基咪唑、乙烯基吡咯烷酮、吡咯烷酮、二乙烯基亚乙基脲和咪唑)的共聚物中发现的杂质
原则
易于在乙烯基吡咯烷酮-乙烯基咪唑共聚物(乙烯基咪唑、乙烯基吡咯烷酮、吡咯烷酮、二乙烯基亚乙基脲和咪唑)中发现的组成单体和/或杂质的检测和确定。
使用氮特异性检测器(NSD)通过毛细管气相色谱法进行分析。要分析的物质预先用丙酮从聚合物中提取出来。
内容范围待定
乙烯基咪唑
2-55微克/克
乙烯吡咯烷酮
2-50微克/克
吡咯烷酮
2-70微克/克
二乙烯基亚乙基脲
2-33微克/克
咪唑
2-50微克/克
3.试剂和参考材料
3.1. Vinylpyrrolidone-vinylimidazole copolymers;
3.2.
3.3.
3.4.
3.5.
3.6.
3.7.
3.8.
4.完成的
4.1. 1.决心
4.2. 【微克/克】
nq*
nd**
钕
2.决心
nq
3.决心
4.决心
5.决心
5.1. 6.决心
平均的
5.2. 标准偏差
柯夫。变异的
5.3. 测量不确定度
相对测量不确定度
*nq =不可量化: **nd=无法检测
在样品中,无法检测到乙烯基吡咯烷酮和二乙烯基亚乙基脲,并且无法定量乙烯基咪唑。
可重复性
用所有分析物补充共聚物样品,然后分析6次。可重复性条件下的准确度可以从乙烯基吡咯烷酮、二乙烯基亚乙基脲和乙烯基咪唑的可重复性中推断出来。(表2) 表2
*=根据迪克森测试的异常值 加成回收
从表2中可以计算出回收率。
注意 对乙烯基吡咯烷酮-乙烯基咪唑的其它共聚物的适用性
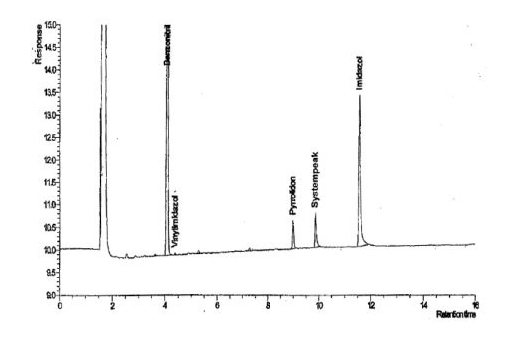
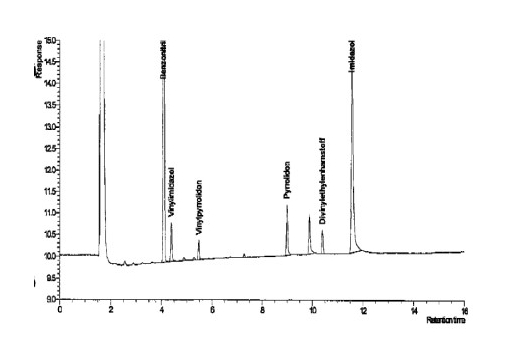
该方法已在Divergan HM中得到验证。原则上,我们可以认为该测定也适用于乙烯基吡咯烷酮-乙烯基咪唑的其他共聚物。 图1:共聚物提取物的色谱图(含内标)
图2共聚物提取物的色谱图(含内标)。
辅以2.1克/克乙烯基咪唑、2.1微克/克乙烯基吡咯烷酮、3.9微克/克吡咯烷酮、2.1克/克二乙烯基亚乙基脲和12.7克/克咪唑。
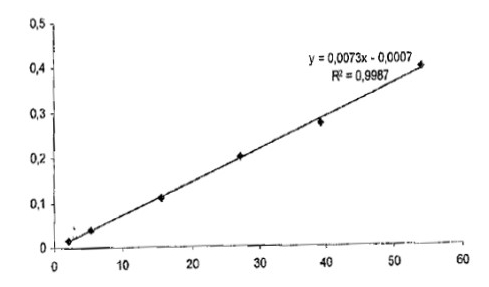
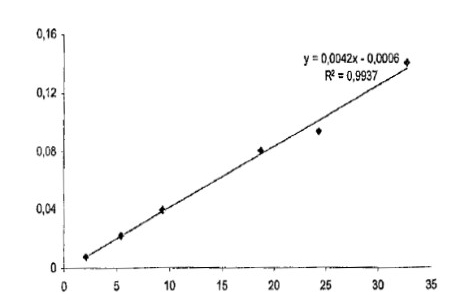
图3:乙烯基咪唑的校准线
分析物峰面积*测试样品(int。std。)
峰面积(整数。std。)【毫克】
与标准测试样品相关的分析物测试样品【g/g】
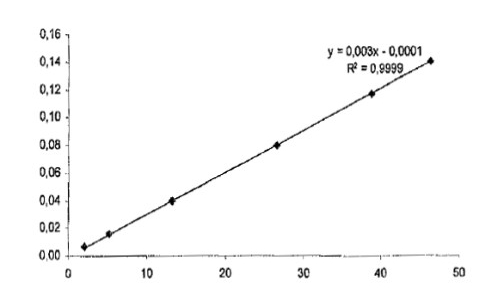
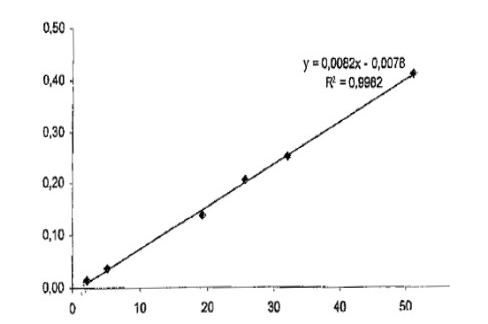
图4:乙烯基吡咯烷酮的校准线
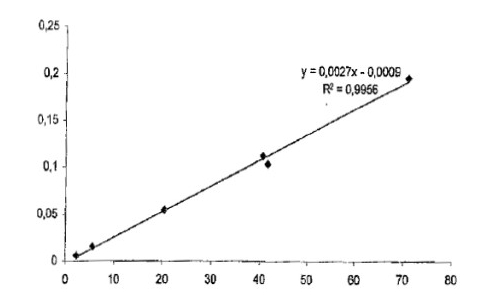
图5:吡咯烷酮的校准线
图6:二乙烯脲的校准线
图7:咪唑的校准线
分析物峰面积*测试样品(int。std。)
7.1. 峰面积(整数。std。)【毫克】
附录2:检测葡萄酒和葡萄汁中咪唑、吡咯烷酮和残留单体(乙烯基吡咯烷酮、乙烯基咪唑、二乙烯基咪唑烷酮)的分析方法
范围
此处描述的方法适用于测定白葡萄酒、红葡萄酒、甜葡萄酒和干葡萄酒以及葡萄汁中的咪唑、吡咯烷酮、乙烯基咪唑和乙烯基吡咯烷酮。
7.2. 二乙烯基咪唑烷酮在pH值为3.7时的半衰期为3.75分钟。因此,在葡萄酒和葡萄汁中进行测定是不合适的。
所述研究涵盖咪唑的浓度范围为5至125微克/升、吡咯烷酮的浓度范围为25至250微克/升、乙烯基咪唑的浓度范围为2至25微克/升、乙烯基吡咯烷酮的浓度范围为2至12.5微克/升。
定义
高效液相色谱
液相色谱-质谱联用仪
MRM:多反应监测
样品直接在反相色谱柱(C18)上通过LC-MS进行分析。然后在多反应监测模式下进行检测。
8.1. 试剂和材料
化学品
CL-SM的甲醇(LiChrosolov)(化学文摘社编号:67-56-1)质量
8.2. 双蒸馏水
七氟丁酸。,≥99.5%(化学文摘社:375-22-4)
洗脱液的制备
溶剂A:
9.1. 用移液管将0.6毫升七氟丁酸(4.1.3)移至1000毫升双蒸水(4.1.2)中,摇晃并脱气。
溶剂B:

将300毫升双蒸水(4.1.2)添加到700毫升甲醇(4.1.1)中并摇晃。用移液管将0.6毫升七氟丁酸(4.1.3)移至该溶液中,摇晃并脱气。
标准0 咪唑,≥99.5%(化学文摘社编号:288-32-4)
吡咯烷酮,≥99 %(化学文摘社编号:616-45-5)0 乙烯基咪唑,≥99 %(化学文摘社编号:1072-63-5)
乙烯基吡咯烷酮= 99.8%(化学文摘社编号:88-12-0) 0 标准溶液的制备储备标准溶液的制备(1,00 g/l):准确称量100 mg标准溶液(4.3.1-4.3.4),将其无损转移至100 ml容量瓶中,用双蒸水(4.1.2)填充至约90 ml,摇晃并调整至100 ml。
混合标准溶液的制备(咪唑:62.5毫克/升;吡咯烷酮:62.5毫克/升;乙烯基咪唑:12.5毫克/升;乙烯基吡咯烷酮:6.25毫克/升); 0 用移液管将6.25毫升咪唑储备溶液(4.4.1)、6.25毫升吡咯烷酮储备溶液(4.4.1)、1.25毫升乙烯基咪唑储备溶液(4.4.1)和0.625毫升乙烯基吡咯烷酮储备溶液(4.4.1)移至100毫升容量瓶中,用双蒸水(4.1.2)填充至约90毫升,摇匀并调整至100毫升。
工作标准溶液的制备:
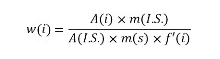
高效液相色谱
液相色谱-质谱联用仪
MRM:多反应监测
样品直接在反相色谱柱(C18)上通过LC-MS进行分析。然后在多反应监测模式下进行检测。
8.1. 试剂和材料
化学品
CL-SM的甲醇(LiChrosolov)(化学文摘社编号:67-56-1)质量
8.2. 双蒸馏水
七氟丁酸。,≥99.5%(化学文摘社:375-22-4)
洗脱液的制备
9.溶剂A:
9.1. 用移液管将0.6毫升七氟丁酸(4.1.3)移至1000毫升双蒸水(4.1.2)中,摇晃并脱气。
溶剂B:
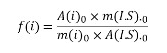
将300毫升双蒸水(4.1.2)添加到700毫升甲醇(4.1.1)中并摇晃。用移液管将0.6毫升七氟丁酸(4.1.3)移至该溶液中,摇晃并脱气。
标准0 咪唑,≥99.5%(化学文摘社编号:288-32-4)
吡咯烷酮,≥99 %(化学文摘社编号:616-45-5)0 乙烯基咪唑,≥99 %(化学文摘社编号:1072-63-5)
乙烯基吡咯烷酮= 99.8%(化学文摘社编号:88-12-0) 0 标准溶液的制备储备标准溶液的制备(1,00 g/l):准确称量100 mg标准溶液(4.3.1-4.3.4),将其无损转移至100 ml容量瓶中,用双蒸水(4.1.2)填充至约90 ml,摇晃并调整至100 ml。
混合标准溶液的制备(咪唑:62.5毫克/升;吡咯烷酮:62.5毫克/升;乙烯基咪唑:12.5毫克/升;乙烯基吡咯烷酮:6.25毫克/升); 0 用移液管将6.25毫升咪唑储备溶液(4.4.1)、6.25毫升吡咯烷酮储备溶液(4.4.1)、1.25毫升乙烯基咪唑储备溶液(4.4.1)和0.625毫升乙烯基吡咯烷酮储备溶液(4.4.1)移至100毫升容量瓶中,用双蒸水(4.1.2)填充至约90毫升,摇匀并调整至100毫升。
工作标准溶液的制备:
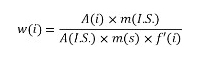
将300毫升双蒸水(4.1.2)添加到700毫升甲醇(4.1.1)中并摇晃。用移液管将0.6毫升七氟丁酸(4.1.3)移至该溶液中,摇晃并脱气。
用移液管将40 l混合标准溶液(4.4.2)移至25 ml容量瓶中,用双蒸水填充至25ml并摇匀。
标准基质校准曲线的制备
乙烯基吡咯烷酮= 99.8%(化学文摘社编号:88-12-0)基质匹配校准溶液在未受污染的葡萄酒或葡萄汁中制备。用样品适当稀释混合标准溶液(4.4.2),得到五种工作标准。
混合标准溶液的制备(咪唑:62.5毫克/升;吡咯烷酮:62.5毫克/升;乙烯基咪唑:12.5毫克/升;乙烯基吡咯烷酮:6.25毫克/升);测量前必须准备好校准标准!
结束音量
混合标准
25毫升
0微升
10.1.0微克/升
10微升
25微克/升
10.2.5微克/升
2.5微克/升
乙烯基咪唑
20微升
乙烯吡咯烷酮
50微克/升
吡咯烷酮
10微克/升
二乙烯基亚乙基脲
30微升
咪唑
75微克/升
10.3.15微克/升
7.5微克/升
乙烯基咪唑
40微升
乙烯吡咯烷酮
40微升
吡咯烷酮
40微升
二乙烯基亚乙基脲
40微升
咪唑
40微升
10.4.100微克/升
20微克/升
50微升
| ||||||
4.1 | 10.7 | |||||
4.3 | 10.8 | |||||
4.2 | 11.5 | |||||
4.3 | 11.8 | |||||
3.9 | 10.2 | |||||
3.9 | 10.8 | |||||
4.1 | 11.0 | |||||
0.2 | 0.6 | |||||
% | 4.8 | 5.1 | ||||
0.6 | 1.7 | |||||
% | 14 | 15 | ||||
10.4.1.
流速:1毫升/分钟 | ||||||
[%] | 102.3 | 112.4 | 97.0 | 103.3 | 90.7 | |
[%] | 98.5 | 101.9 | 89.6 | 102.1 | 91.7 | |
[%] | 111.8* | 111.5 | 105.7 | 111.1 | 112.6* | |
[%] | 102.7 | 103.3 | 91.9 | 104.8 | 94.5 | |
[%] | 104.2 | 101.0 | 89.3 | 102.7 | 97.0 | |
[%] | 100.4 | 104.9 | 90.4 | 110.3 | 95.4 | |
[%] | 101.6 | 105.8 | 94.0 | 105.7 | 93.9 | |
[%] | 2.2 | 4.9 | 6.4 | 3.9 | 2.6 | |
[%] | 2.2 | 4.7 | 6.8 | 3.7 | 2.8 | |
[%] | 6.6 | 14.8 | 19.2 | 11.8 | 7.8 | |
[%] | 7 | 14 | 20 | 11 | 8 | |
渐变:
10.5.色谱柱加热器:25℃
运行时间:45分钟
乙烯基咪唑
101.6 %
乙烯吡咯烷酮
105.8 %
吡咯烷酮
94.0 %
二乙烯基亚乙基脲
105.7 %
咪唑
93.9 %
MS条件:
质谱仪
应用生物系统API 4000或同等标准
扫描类型
极性 机械去骨肉
积极的
离子源
涡轮喷雾
持续时间
20,005分钟;1364次循环
离子源
涡轮喷雾
持续时间
窗帘气体
离子源
涡轮喷雾
持续时间
40磅/平方英寸
离子源
涡轮喷雾
持续时间
离子喷雾电压
2500伏
温度
持续时间
550摄氏度
1.离子源气体1
60磅/平方英寸
离子源气体2:
碰撞气体
中等
入口电势
10伏
衣领2
原则
复合的
Q1弥撒
4.1. Q3质量(amu)
4.1.1. 停留时间(毫秒)
4.1.2. 参数
4.1.3. 开始
4.2. 停止
4.2.1. 数据处理
英国国教会
CXP
去聚集电位(单位:伏特)
碰撞能量(伏特)
碰撞单元出口电势(单位:伏特)
估价
标识:
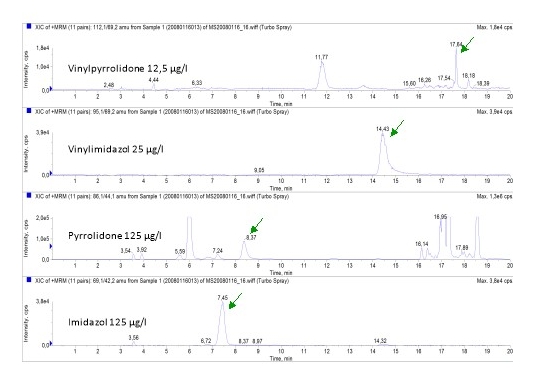
注入10 μl工作标准溶液(4.4.3)以确定保留时间。大约保留时间为:
保留时间
7.45分钟
8.37分钟
4.4.2. 14.43分钟
17.64分钟
4.4.3. 量化:
定量质量转移:
4.5. 质量传递
69.1 → 42.2
86.1 → 44.1
级数的平均值
标准偏差
相应的CV
霍维茨相对标准偏差%
实验室内再现性(SD
walter 沃尔特
40微克/升
60微克/升
80微克/升
重复性(标准偏差
6.1. 恢复(WDF):
8微克/升
16微克/升
6.2. 4微克/升
密苏里催化剂公司
因此
6.3. + 49.8%不适用
+ 0.3%硫酸铜
)、默克、达姆施塔特或同等产品
上限的计算基于从迁移试验中获得的结果,推荐剂量为0.5g/l,最长施用时间为48小时,处理温度为20°C,乘以系数2。
在酸性条件下(pH值较低时),二乙烯基咪唑烷酮(二乙烯基乙烯脲)不稳定,因此会降解为咪唑啉酮和乙烯醇。此外,咪唑啉酮降解为尿素和乙二醇。乙烯醇与乙醛处于化学平衡状态。
除乙醛、尿素和乙二醇外,咪唑啉酮也被纳入毒理学评估。
页脚菜单
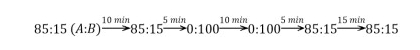
7.2.
Ion Source | Turbo Spray |
Duration | 20,005 min; 1364 Cycles |
Curtain Gas | 40 psi |
Ionspray Voltage | 2500 V |
Temperature | 550°C |
Ion Source Gas 1 | 60 psi |
Ion Source Gas 2: | 60 psi |
Collision Gas | Medium |
Entrance Potential | 10 V |
Collar 2 | 0 |
compound | Q1 Mass (amu) | Q3 mass (amu) | Dwell (msec) | Parameter | Start | Stop |
69.08 | 42.20 | 75.00 | DP | 81.00 | 81.00 | |
CE | 31.00 | 31.00 | ||||
CXP | 2.00 | 2.00 | ||||
86.10 | 44.10 | 75.00 | DP | 66.00 | 66.00 | |
CE | 31.00 | 31.00 | ||||
CXP | 6.00 | 6.00 | ||||
86.10 | 69.00 | 75.00 | DP | 66.00 | 66.00 | |
CE | 23.00 | 23.00 | ||||
CXP | 4.00 | 4.00 | ||||
95.09 | 41.10 | 75.00 | DP | 71.00 | 71.00 | |
CE | 33.00 | 33.00 | ||||
CXP | 0.00 | 0.00 | ||||
95.09 | 69.20 | 75.00 | DP | 71.00 | 71.00 | |
CE | 29.00 | 29.00 | ||||
CXP | 12.00 | 12.00 | ||||
112.08 | 69.20 | 75.00 | DP | 51.00 | 51.00 | |
CE | 21.00 | 21.00 | ||||
CXP | 4.00 | 4.00 | ||||
112.08 | 84.00 | 75.00 | DP | 51.00 | 51.00 | |
CE | 17.00 | 17.00 | ||||
CXP | 14.00 | 14.00 |
DP | Declustering Potential (in volts) |
CE | Collision Energy (in volts) |
CXP | Collision Cell Exit Potential (in volts) |
Evaluation
Identification:
Inject 10 μl of working standard solution (4.4.3) to ascertain the retention times. Approximate retention times are:
compound | retention time |
7.45 min | |
8.37 min | |
14.43 min | |
17.64 min |
8.2. Quantification:
Mass transfers for quantification:
compound | mass transfer |
69.1 → 42.2 | |
86.1 → 44.1 | |
95.1 → 69.2 | |
112.1 → 69.2 |
Use the standard addition method for quantification.
8.3. Expression of results
Results should be expressed in μg/l for Imidazole, Pyrrolidone, Vinylimidazole and Vinylpyrrolidone with no decimals (e.g. 3 μg/l).
8.4. Limit of detection and limit of quantification
The limit of detection (LOD) and the limit of quantification (LOQ) depend on the individual measurement conditions of the chemical analysis and are to be determined by the user of the method.
The limit of detection (LOD) and the limit of quantification were estimated using the instrumentation and conditions mentioned as an example above (section 7) following the instructions in the resolution OENO 7-2000 (E-AS1-10-LIMDET) “Estimation of the Detection and Quantification Limits of a Method of Analysis“. Following the "Logic Diagram for Decision-Making" in point 3 the "graph" approach should be applied following paragraph 4.2.1. For this purpose a window is drawn on the multiple reaction monitoring chromatogram, enclosing the range of a tenfold peak width at mid-height (w½) either side at the retention time of an analyte peak in the relevant part of the chromatogram. Two parallel lines are then drawn which just enclose the maximum amplitude of the signal window. The separation between these two lines gives hmax, expressed in abundance units, which is multiplied by 3 for LOD, by 10 for LOQ, and finally converted into concentration units by implementing the individual response factor.
compound | limit of detection (LOD) | limit of quantification (LOQ) |
12 μg/l | ||
83 μg/l | ||
2 μg/l | 6 μg/l | |
2 μg/l | 6 μg/l | |
Precision and trueness
As matrices three different wines (dry white wine, dry red wine and sweet red wine) and grape juice were used. Within-laboratory reproducibility, repeatability and recovery were calculated based on matrix calibration and three spikes (Imidazole: 40/60/80 μg/l; 2-Pyrrolidone: 40/60/80 μg/l; Vinylimidazole: 8/12/16 μg/l; Vinylpyrrolidone: 4/6/8 μg/l).
9.1.
fortification | mean of series | standard deviation | corresponding CV | Horwitz RSD % | |||
within-laboratory reproducibility (SDwlR): | 40 μg/l | 41 | 2 | 5 | % | 26 | |
60 μg/l | 61 | 3 | 5 | % | 24 | ||
80 μg/l | 80 | 5 | 6 | % | 23 | ||
repeatability (SDr): | 40 μg/l | 41 | 1 | 2 | % | ||
60 μg/l | 61 | 2 | 3 | % | |||
80 μg/l | 80 | 4 | 5 | % | |||
recovery (WDF): | 40 μg/l | 102 | % | ||||
60 μg/l | 101 | % | |||||
80 μg/l | 101 | % | |||||
0 | 101 | % | |||||
fortification | mean of series | standard deviation | corresponding CV | Horwitz RSD % | |||
within-laboratory reproducibility (SDwlR): | 40 μg/l | 42 | 9 | 22 | % | 26 | |
60 μg/l | 60 | 9 | 15 | % | 24 | ||
80 μg/l | 81 | 9 | 11 | % | 23 | ||
repeatability (SDr): | 40 μg/l | 42 | 5 | 12 | % | ||
60 μg/l | 60 | 4 | 7 | % | |||
80 μg/l | 81 | 8 | 9 | % | |||
recovery (WDF): | 40 μg/l | 105 | % | ||||
60 μg/l | 100 | % | |||||
80 μg/l | 101 | % | |||||
0 | 102 | % | |||||
9.2.
fortification | mean of series | standard deviation | corresponding CV | Horwitz RSD % | |||
within-laboratory reproducibility (SDwlR): | 8 μg/l | 8 | 0 | 4 | % | 33 | |
12 μg/l | 12 | 1 | 5 | % | 31 | ||
16 μg/l | 16 | 1 | 4 | % | 30 | ||
repeatability (SDr): | 8 μg/l | 8 | 0 | 4 | % | ||
12 μg/l | 12 | 0 | 3 | % | |||
16 μg/l | 16 | 0 | 3 | % | |||
recovery (WDF): | 8 μg/l | 101 | % | ||||
12 μg/l | 102 | % | |||||
16 μg/l | 102 | % | |||||
0 | 102 | % | |||||
9.3.
fortification | mean of series | standard deviation | corresponding CV | Horwitz RSD % | |||
within-laboratory reproducibility (SDwlR): | 4 μg/l | 3 | 1 | 31 | % | 37 | |
6 μg/l | 4 | 1 | 26 | % | 35 | ||
8 μg/l | 5 | 2 | 29 | % | 33 | ||
repeatability (SDr): | 4 μg/l | 3 | 1 | 25 | % | ||
6 μg/l | 4 | 1 | 22 | % | |||
8 μg/l | 5 | 1 | 26 | % | |||
recovery (WDF): | 4 μg/l | 66 | % | ||||
6 μg/l | 63 | % | |||||
8 μg/l | 66 | % | |||||
0 | 65 | % | |||||
[1]
Missouri Catalyst (= 49.9% K2SO4 + 49.8% Na2SO4 + 0.3% CuSO4), Merck, Darmstadt or the equivalent
[2] The calculation of the upper limits was based on the results obtained from the migration tests with the recommended dosage of 0,5 g/l, the maximum application time of 48 hours, and a treatment temperature of 20 °C, multiplied by a factor of 2.
Under acidic conditions (at lower pH-values) divinylimidazolidinone (divinylethylene-urea) is not stable and hence degrades to imidazolidinone and vinyl alcohol. Furthermore imidazolidinone degrades to urea and ethylene glycol. Vinyl alcohol is in chemical equilibrium with acetaldehyde.
Imidazolidinone was included in the toxicological assessment as well as acetaldehyde, urea and ethylene glycol.


